El Instituto de Neurociencias da un nuevo paso para comprender el funcionamiento de las células madre del cerebro adulto
Investigadores de este centro, perteneciente a la Universidad de Elche y al Consejo Superior de Investigaciones Científicas, consiguen comprender el mecanismo que lleva a las células totipotenciales a permanecer como tales o desarrollarse como neuronas

Los investigadores Ángela Nieto y Joan Garcelán, en el Instituto de Neurociencias / INFORMACIÓN / Información
El Instituto de Neurociencias (IN), uno de los centros de referencia internacional en la investigación del cerebro y el sistema nervioso asentado en la provincia de Alicante, ha dado un nuevo paso en la comprensión del funcionamiento de las células madre en el cerebro adulto. Las células madre pueden mantenerse como tales o pueden generar neuronas. Lo que no se conocía era cómo se resolvía en la célula la decisión de seguir siendo una célula madre o convertirse en neurona. Hasta ahora.
"Conflicto"
Investigadores del laboratorio de Plasticidad Celular en Desarrollo y Enfermedad, que dirige Ángela Nieto en el Instituto de Neurociencias, centro mixto del Consejo Superior de Investigaciones Científicas (CSIC) y la Universidad Miguel Hernández (UMH) de Elche y cuya sede está en el campus de Sant Joan d'Alacant, han descubierto el mecanismo que permite a las células madre del cerebro adulto expresar tanto los genes de mantenimiento de su identidad como los de diferenciación neuronal sin que se produzcan conflictos en la actividad celular. Además, este mecanismo permite que las células madre estén preparadas para diferenciarse rápidamente.
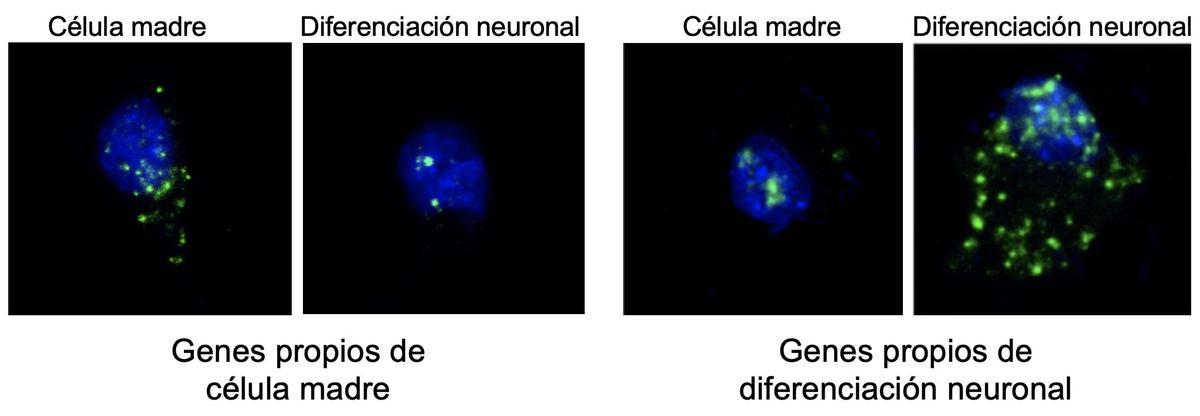
Mecanismo de funcionamiento de células madre en el cerebro / Información
Identidad celular
Todas las células de un organismo tienen los mismos genes, pero la diferencia entre unas y otras está en los genes que expresan y los que no. Esto es lo que se conoce como identidad celular y va a determinar las funciones de las células a lo largo de su vida.
El caso de las células madre cerebrales es muy particular porque expresan los genes que las mantienen como células madre, pero también expresan otros genes que son propios de las neuronas que producen.
Hasta el momento, se desconocía cómo era posible que, a pesar de expresar ambos tipos de genes, se evitara lo que se conoce como un conflicto de decisión, es decir, que la célula no entienda si se debe convertir en una neurona o si se debe mantener como una célula madre.
Sin embargo, los resultados de este estudio, publicado recientemente en la revista Nature Communications, han desvelado el mecanismo que previene que los genes de diferenciación se traduzcan en las células madre, resolviendo así el supuesto problema del conflicto de decisiones en las actividades de las distintas células.
La importancia de quedarse dentro o salir del núcleo de la célula
“Cuando los genes se transcriben, generan ARN mensajeros que luego se traducen en proteínas, las efectoras de las funciones celulares. Para que este proceso se produzca se requiere que esos mensajeros salgan del núcleo de la célula y vayan al citoplasma para traducirse correctamente”, apunta Ainara González-Iglesias, primera autora del artículo publicado en la mencionada revista científica.
Los expertos descubrieron que la clave está en que los ARN mensajeros de los genes de las células madre salían del núcleo para traducirse a proteínas, mientras que los mensajeros de los genes neuronales se quedaban retenidos en el núcleo. “Por ello las células seguían manteniendo su condición de células madre”, explica la investigadora.
Un interruptor de doble sentido
Cuando las células madre deben diferenciarse para dar lugar a neuronas, el mecanismo funciona de la misma manera. Nieto explica que, en ese caso, “son los mensajeros de los genes de mantenimiento de células madre los que se quedan retenidos en el núcleo y, por lo tanto, no pueden traducirse a proteínas y realizar su función”.
Aunque ambos tipos de genes estén expresados en cada momento, “siempre se quedan retenidos los mensajeros de los que no tienen que funcionar”, destaca la investigadora, al tiempo que hace hincapié en que este mecanismo, no solo ayuda a las células a no tener un conflicto de decisión, sino que, además, "permite tener la maquinaria preparada para poder diferenciarse inmediatamente en cuanto reciben la señal para hacerlo”.
Las células madre tienen la capacidad de regenerar tejidos y, a pesar de que en el caso del cerebro humano no se sabe a ciencia cierta hasta qué punto contribuyen a la regeneración cerebral en el adulto, la investigadora señala que el correcto funcionamiento de este mecanismo es fundamental, porque de lo contrario podría producirse una diferenciación neuronal prematura, que dificultaría el adecuado funcionamiento del sistema nervioso.
Colaboración nacional
Esta investigación se ha realizado con la colaboración del laboratorio que dirige Isabel Fariñas, experta en células madre, en el Instituto de Biotecnología y Biomedicina de la Universidad de Valencia y del laboratorio que dirige Juan Valcárcel, experto en mecanismos de procesamiento del ARN, en el Centro de Regulación Genómica de Barcelona. Para llevarla a cabo, los investigadores han estudiado la zona subventricular del cerebro del ratón adulto, ya que se trata de una región que presenta una población muy amplia de células madre. Estudiando esa zona pudieron comprobar que el mecanismo de retención en el núcleo "tiene que ver con la falta de una modificación del ARN que se llama metilación, que induce la eliminación de los intrones, unos fragmentos del ARN mensajero que deben eliminarse para que salgan del núcleo y se traduzcan las proteínas", según se recoge en una nota de prensa del CSIC.
A través de la hibridación in situ, una técnica que permite ver el ARN mensajero en el tejido mediante el uso de sondas marcadas, los expertos fueron capaces de observar en detalle cómo el ARN mensajero quedaba retenido en el núcleo.
Fue precisamente el uso de esta técnica, ampliamente utilizada en el laboratorio que dirige Nieto en el IN, lo que permitió a los investigadores identificar el mecanismo completo: “Aunque ahora hay técnicas de secuenciación más modernas, si no hubiéramos utilizado la hibridación in situ, no hubiéramos detectado lo que estaba sucediendo en el núcleo de las células”, cuenta González-Iglesias.
Financiación
Este trabajo ha sido posible gracias a la financiación del Ministerio de Ciencia, Innovación y Universidades, el Instituto de Salud Carlos III, los Programas ISIC y PROMETEO de la Generalitat Valenciana, el Ministerio de Educación, Cultura y Deportes, el Programa Severo Ochoa para Centros de Excelencia en Investigación y Desarrollo de la Agencia Estatal de Investigación, el Consejo Europeo de Investigación (ERC) y el Programa CERCA de la Generalitat de Catalunya.
- PP y Vox cambian el reglamento municipal del bilingüismo para "equiparar" castellano y valenciano en Elche después de 27 años
- La Policía Local de Santa Pola auxilia, reanima y traslada al centro de salud a un bebé que perdió la consciencia
- La plataforma por la reversión del Vinalopó quiere rodear el hospital con una cadena humana
- Pablo Ruz: "Es necesario que el Obispado tenga más proactividad con Santa María
- Detenidos un padre y un hijo en Elche por simular el robo de una consola, un televisor y ropa exclusiva para cobrar del seguro
- Ruz cambia el paso, aspira a liderar un movimiento social para buscar fondos para Santa María y convoca un pleno
- La caída de cascotes obliga a acordonar la Puerta Mayor de la basílica de Santa María
- La ampliación del Parque Empresarial encara su recta final con una modificación para abaratar el suelo